Azepan
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
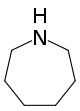
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Azepan | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H13N | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit aminartigem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 99,18 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,86 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
135–138 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
mischbar mit Wasser[1] | |||||||||||||||
| Brechungsindex |
1,4631 (20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Azepan ist eine gesättigte heterocyclische chemische Verbindung. Sie ist der einfachste siebengliedrige stickstoffhaltige Heterocyclus und wird auch häufig als Hexamethylenimin bezeichnet. Diese Bezeichnung ist allerdings etwas irreführend, denn es handelt sich nicht um ein Imin im (heutigen) eigentlichen Sinne. Eine weitere Bezeichnung ist Homopiperidin, da es sich um ein Homologes des Piperidins, das um eine Methylengruppe erweitert ist, handelt.
Herstellung
[Bearbeiten | Quelltext bearbeiten]Die Synthese von Azepan kann durch Reduktion von ε-Caprolactam mit Lithiumaluminiumhydrid[3] oder Natriumborhydrid[4] durchgeführt werden. Auch die Cyclisierung von 1,6-Diaminohexan beispielsweise am Rutheniumkatalysator (in diesem Fall Tris(triphenylphosphino)dichlororuthenat(II)) stellt einen Syntheseweg dar.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Azepan ist eine farblose Flüssigkeit mit ammoniakartigem Geruch. Sie ist vollständig mischbar mit Wasser. Es handelt sich um eine Stickstoffbase. Ihr pKs-Wert in Wasser beträgt bei 20 °C 11,4.[6]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i Eintrag zu Hexamethylenimin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-280.
- ↑ L. Ruzicka, M. Kobelt, O. Hafliger, V. Prelog in: Helvetica Chimica Acta 1949, 32, 544–552.
- ↑ S. R. Wann, P. T. Thorsen, M. M. Kreevoy in: J. Org. Chem. 1981, 46, 12, 2579–2581.
- ↑ Bui-The-Khai, C. Concilio, G. Porzi in: J. Org. Chem. 1981, 46, 8, 1759–1760.
- ↑ D. Yang, G. Zuccarello, B. R. Mattes in: Macromolecules 2002, 35, 13, 5304–5313.


